Ricercando nella letteratura scientifica mondiale, in merito ai tanti argomenti che riguardano la panificazione, mi sono imbattuta in un altro interessante studio, argomento tra l’altro, spesso dibattuto anche dagli operatori amatoriali.
Il pane si realizza con la farina e le farine sono il frutto della macinazione di tante varietà di grano. Ci chiediamo e vi chiederete – cosa possiamo mai saperne di test sul grano? – Acquistiamo la nostra bella farina e con lei facciamo il pane. Al primo colpo un pane forse non riesce subito come si spera ma al secondo, sicuramente anche al terzo, ci si avvicina a qualcosa che può essere chiamato Pane.
Le etichette presenti sulle farine non ci aiutano davvero e molte persone (io ero una di quelle), non sanno nemmeno che una farina dispone di una scheda tecnica sulla quale c’è scritto “qualcosa” che per lo più, è di abbastanza difficile traduzione. – Cosa fai dunque? – Se sei davvero cocciuto e curioso e vuoi imparare qualcosa ti immergi nelle letture (non sono certo le letture di un blog qualsiasi perché è tutto ciò che vi trovo scritto è un “riporto” di nozioni abbastanza confuse e così, ti ritrovi a notte inoltrata a cercare di trovare spunti seri.
Una delle più frequenti domande è – ma cosa ci mettono dentro la farina? – La risposta è sempre molto approssimativa e rispecchia una mia convinzione: ci lanciamo in test e miscele, la annacquiamo, ci compriamo le pentole contenitive perché il pane altrimenti si “siede”, ci attacchiamo con il naso al forno ogni volta che assistiamo alla trasformazione dalla massa cruda a cotta e dal colore marron dorato che ricorda il sole a mezzo tramonto ma……in un modo o in un altro, avremmo bisogno di qualche certezza e…non c’è! Dobbiamo affidarci a quella magia che trasforma la polvere bianca, gialla o bruna, in quel prodotto fragrante e croccante dal profumo inebriante che è il PANE, con le sole nostre forze perché la “ricetta perfetta” non c’è!
Ci sono tanti pani, tanti stili, tante scuole di pensiero, tanto di tutto ma l’unica certezza siamo noi che SOLO a forza di studiare potremo realizzare il nostro prodotto! E allora vogliamo studiare…
L’uso di enzimi nell’idrolisi dell’amido
L’amido è il carboidrato di stoccaggio più comune presente nelle piante. È usato dalle piante stesse, dai microbi e dagli organismi superiori, quindi, esiste una grande diversità di enzimi in grado di catalizzare la sua idrolisi. L’amido di tutte le fonti vegetali si presenta sotto forma di granuli che differiscono notevolmente per dimensioni e caratteristiche fisiche, da specie a specie.
Le differenze chimiche sono meno marcate.
La principale differenza è il rapporto tra amilosio e amilopectina. Ad esempio, l’amido di mais ceroso contiene solo il 2% di amilosio, ma quello dell’amiloma è di circa l’80% di amilosio. Alcuni amidi, ad esempio quello della patata, contengono fosfato legato in modo covalente in piccole quantità (circa lo 0,2%), che ha effetti significativi sulle proprietà fisiche dell’amido, ma non interferisce con la sua idrolisi.
L’idrolisi acida dell’amido ha avuto in passato, un uso significativo. Oggi è in gran parte sostituita dai processi enzimatici. Poiché richiedeva l’uso di materiali resistenti alla corrosione, ha dato origine ad un elevato contenuto di colore e sali di sodio (dopo la neutralizzazione) che necessitando di più energia per il riscaldamento, era relativamente difficile da controllare.
L’amilopectina presenta la grande sfida ai sistemi idrolitici enzimatici. Ciò è dovuto ai residui coinvolti nei punti di ramificazione che costituiscono circa 4-6% del glucosio presente. La maggior parte degli enzimi idrolitici sono specifici e devono essere distrutti per una completa idrolisi che trasforma l’amilopectina in glucosio. Alcuni degli ultimi studi più incisivi nello sviluppo di nuovi enzimi hanno riguardato gli enzimi deramificati.
È necessario idrolizzare l’amido in un’ampia varietà di processi i quali possono essere raggruppati in due classi fondamentali:
- processi in cui l’amido idrolizzato deve essere usato dai microbi o dall’uomo
- processi in cui è necessario eliminare l’amido.
Nei processi primari come nella produzione dello sciroppo di glucosio, l’amido è solitamente il componente principale, mentre nei processi secondari, come la lavorazione del succo di canna da zucchero, piccole quantità di amido che contaminano i materiali non amidacei vengono rimosse. In questi processi sono coinvolti enzimi di vario tipo e sebbene sia possibile utilizzare amidi provenienti da diverse piante, il mais è la fonte più abbondante a livello mondiale e fornisce la maggior parte del “substrato” utilizzato nella preparazione degli idrolizzati.
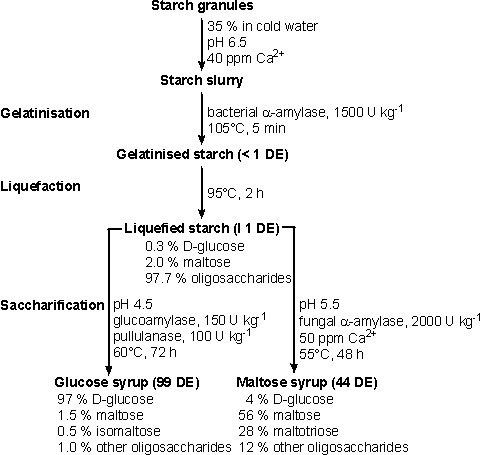
Nella conversione dell’amido si distinguono tre fasi:
- Gelatinizzazione – che comporta la dissoluzione dei granuli di amido di dimensioni nanogrammi per formare una sospensione viscosa;
- Liquefazione, che comporta l’idrolisi parziale dell’amido, con concomitante perdita di viscosità;
- Saccarificazione, che comporta la produzione di glucosio e maltosio mediante ulteriore idrolisi.
La gelatinizzazione è ottenuta riscaldando l’amido con acqua. Questa condizione si verifica necessariamente e naturalmente quando gli alimenti amidacei vengono cotti. Se ad esempio versiamo dell’acqua sufficientemente calda sulla farina, otteniamo la gelatinizzazione dell’amido (vedi anche tang zhong o roux). L’amido gelatinizzato è prontamente liquefatto dalla idrolisi parziale mediante enzimi o acidi e viene saccarificato da un’ulteriore idrolisi acida o enzimatica.
L’industria dell’amido e dello sciroppo di glucosio, per descrivere i suoi prodotti, utilizza l’espressione destrosio equivalente (DE), simile nella definizione alle unità di DH (proteolisi), dove:
![]()
Le due espressioni sono simili ma non identiche
![]()
DE rappresenta quindi la percentuale idrolitica dei collegamenti glicosidici (legami covalenti) presenti. Il glucosio puro ha un DE (destrosio equivalente) di 100, il maltosio puro ha un DE di circa 50 (a seconda dei metodi analitici usati nella seconda equazione) e l’amido ha un DE effettivamente pari a zero.
Durante l’idrolisi dell’amido, DE indica la misura di rottura dell’amido. L’idrolisi acida dell’amido è stata a lungo utilizzata per produrre “sciroppi di glucosio” e persino glucosio cristallino (destrosio monoidrato). Quantità considerevoli di sciroppi DE (42 ) sono vengono prodotti utilizzando idrolisi acida e vengono sfruttati in molte applicazioni che riguardano il settore della pasticceria. Ulteriore idrolisi acide non hanno portato a benefici a causa della degradazione di prodotti indesiderabilmente colorati e aromatizzati per cui sembra essere un processo totalmente casuale che non è influenzato dalla presenza di legami glicosidici.
La nomenclatura degli enzimi utilizzati commercialmente per l’idrolisi dell’amido è alquanto confusa e il parametro aggrega talvolta enzimi con attività sottilmente diverse tra loro. Per esempio, una a-amilasi può essere classificata come amilasi liquefacente o saccarificante ma anche questa classificazione risulta inadeguata per definire tutti gli enzimi che vengono usati nell’idrolisi dell’amido commerciale. Una ragione della confusione nella nomenclatura enzimatica è l’impiego della forma anomerica del gruppo riducente rilasciata nel prodotto stesso, piuttosto che quella del legame idrolizzato. I prodotti derivanti da amilasi batteriche e fungine derivano comunque tutti da idrolisi enzimatica di α e β amilasi.
Gli enzimi commerciali utilizzati per l’idrolisi enzimatica industriale dell’amido sono prodotti derivanti da Bacillus amyloliquefaciens (forniti da vari produttori) e da Bacillus licheniformis (Termamyl).
Questi ultimi, venduti i forma liquida, si distinguono principalmente per la loro tolleranza alle alte temperature dove in presenza di amido, alcuni enzimi restano attivi fino a 110°C.
Il massimo DE ottenibile, utilizzando l’attività amilasica, è circa 40 ppm e il trattamento prolungato, porta alla formazione di maltulosio, resistente all’idrolisi.
I valori DE di 8-12 sono utilizzati nella maggior parte dei processi commerciali dove si rende necessaria un’ulteriore saccarificazione. Il requisito principale della liquefazione enzimatica è quello di ridurre la viscosità dell’amido gelatinizzato per facilitare la successiva lavorazione dei prodotti.
L’amido granulare viene invece polverizzato al 30-40% (p/p) con acqua fredda; ad un pH 6,0-6,5, contiene 20-80 ppm (parti per milione) di Ca 2+ che stabilizza e attiva l’enzima che viene aggiunto tramite una pompa dosatrice.
L’α-amilasi viene solitamente somministrata ad alte attività così che la dose di enzima sia corrispondente a circa 1500 U kg ¯¹ pari a 2.490810299E-24 di sostanza secca di amido. Quando viene utilizzato il prodotto Termamyl, la sospensione di amido più l’enzima viene pompata continuamente attraverso una pompa a getto caldo riscaldato a 105°C mediante vapore. La gelatinizzazione avviene quindi molto rapidamente e l’attività enzimatica, combinata con le significative forze di taglio, inizia il processo di idrolisi. Il tempo di permanenza nel fornello a getto è molto breve: l’amido parzialmente gelatinizzato viene trasferito in una serie di tubi di mantenimento a 100-105°C dove permane per 5 minuti nell’attesa di completare il processo di gelatinizzazione. L’idrolisi viene così completata in serbatoi di contenimento a 90-100°C per 1-2 ore. Questi serbatoi contengono deflettori per scoraggiare la retrogradazione. Processi simili possono essere usati con i B. amyloliquefaciens α-amilasi tuttavia non deve essere superatala temperatura massima di 95°C. L’inconveniente è di dover introdurre una ulteriore fase di “cottura” finale, ovvero quando è stata raggiunta la DE necessaria per gelificare i grani di amido refrattari alla rottura, presenti in alcuni tipi di amido che altrimenti causerebbero nebulosità nelle soluzioni finali.
L’amido liquefatto è solitamente saccarificato, ma quantità relativamente modeste, vengono essiccate a spruzzo per essere poi vendute come “maltodestrine” per l’industria alimentare, principalmente per l’impiego di “agenti di carica” negli alimenti per l’infanzia. In questo caso, l’attività enzimatica residua può essere distrutta verso la fine del periodo di riscaldamento, abbassando il pH.
Anche l’α-amilasi fungina trova impiego nell’industria della panificazione. Spesso viene aggiunta alle farine per consentire la produzione di pane e per promuovere la modifica dell’amido durante la fermentazione e un’adeguata formazione di gas.
Ciò è diventato necessario per ll’insorgenza delle mietitrebbiatrici che riducono il tempo tra il taglio e la trebbiatura del grano. In precedenza era sufficiente consentire un germinazione limitata, aumentando la quantità di enzimi endogeni.
Gli enzimi fungini vengono impiegati piuttosto che quelli derivanti dai batteri poiché la loro azione è più semplice da controllare a causa della loro relativa labilità al calore e denaturazione rapida durante la cottura.
Da tutto questo si traggono numerosi spunti anche per noi che panifichiamo a livello amatoriale perché, seppure inconsapevolmente, abbiamo a che fare ogni giorno con gli impasti che, al loro interno, svolgono numerosi di questi processi.
Fonte: http://www1.lsbu.ac.uk/water/enztech/starch.html#tab4_2


